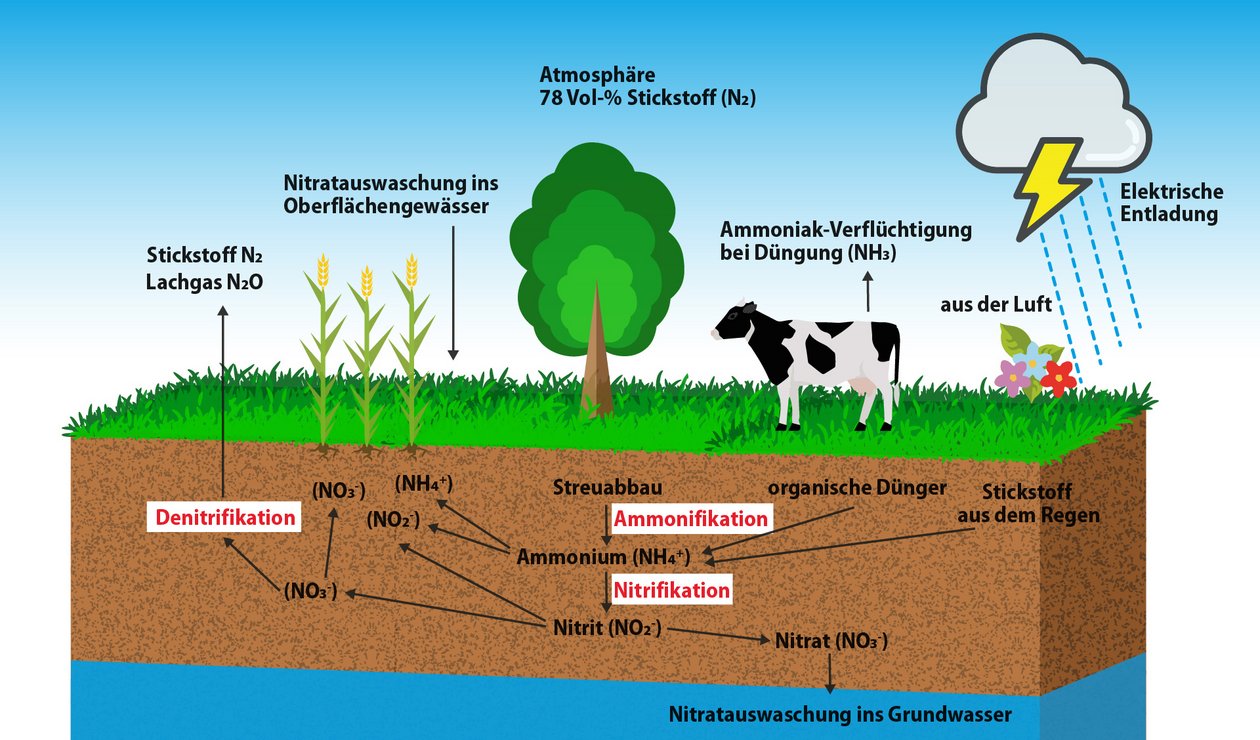
Der Stickstoffkreislauf
In unseren Böden ist Stickstoff von Natur aus ein rares Element und alles Pflanzenwachstum hätte rasch ein Ende, wenn das kostbare Element nicht immer wieder verwertet würde. Lebewesen und Pflanzen nehmen Stickstoff während ihrer Entwicklung aus dem Boden auf und geben ihn nach dem Absterben wieder ab. Die gewaltige Reserve an molekularem Stickstoff in unserer Atmosphäre spielt für diesen Kreislauf kaum eine Rolle. Eher sind es andere – meist nur in Spuren vorkommende – Bestandteile unserer Luft, die in den Kreislauf des Stickstoffs eingreifen. Dieser erfolgt über verschiedene Stufen.
Nur eine kleine Anzahl an Mikroorganismen kann den gewaltigen Stickstoffvorrat in der Erdatmosphäre direkt nutzen. Erst der Mensch hat Wege gefunden, große Massen an Luftstickstoff nutzbar zu machen.
Auf folgenden Wegen wird Luftstickstoff für Pflanzen verfügbar:
- Symbiontische Stickstofffixierung durch Leguminosen in Symbiose mit Knöllchenbakterien (>200 kg/ha Stickstoff im Jahr)
- Nicht symbiontische Stickstofffixierung durch freilebende Mikroorganismen (5 – 15 kg/ha Stickstoff im Jahr)
- Elektrische Entladung bei Blitzschlag (20 – 25 kg/ha Stickstoff im Jahr)
Ammoniaksynthese durch großtechnische Verfahren, mineralische Düngemittel.
Ammonifikation
Aus organischen Stickstoffverbindungen wird durch Bakterien und Pilze Ammonium gebildet. In diesem Prozess wird Stickstoff aus komplexen (und nicht pflanzenverfügbaren) organischen Verbindungen herausgelöst und in eine (nicht nur für Pflanzen attraktive) mineralische Stickstoffspezies umgewandelt.
In vergleichbarer Weise wird Harnstoff via Harnstoffhydrolyse unmittelbar nach der Düngung in Ammoniumstickstoff umgewandelt, wobei zum Teil auch Ammoniak als Endprodukt entstehen kann. Die enzymatische Harnstoffhydrolyse gehört dabei zu den schnellsten Umsetzungsprozessen in der Biologie.
Nitrifikation
Bei der Nitrifikation wird Ammoniumstickstoff (NH4-N) in einem zweistufigen Prozess in Nitrit (NO2-N) und anschließend in das ebenfalls sehr gut pflanzenverfügbare Nitrat (NO3-N) umgewandelt.
NH4+-N (Ammonium) –► NO2--N (Nitrit) –► NO3--N (Nitrat)
Stufe 1 (zum Beispiel Nitrosomonas): NH4+-N + 1½ O2 –► NO2--N + H2O + 2H+
Stufe 2 (zum Beispiel Nitrobacter): NO2--N + ½ O2 –► NO3--N
Die Umwandlung vom Ammonium zum Nitrat erfolgt in mehreren Stufen. Zuerst wird das Ammonium durch Bakterien der Gattung Nitrosomonas zu Hydroxylamin (NH2OH) oxidiert. Möglich wird diese Oxidation durch das Wirken des Enzyms Ammonium-Mono-Oxygenase (AMO). Unter Wirkung des Enzyms Hydroxylamin-Oxidoreduktase (HAO) entsteht aus dem Hydroxylamin Nitrit. Dieses wird schließlich durch Bakterien der Gattung Nitrobacter zu Nitrat oxidiert. Bei dem Prozess werden Protonen frei, die im Boden neutralisiert werden müssen. Bei fortwährenden Nitrifikationsprozessen weisen Böden von Natur aus einen Trend zur Versauerung auf, da jede Umwandlung eines Ammonium- in ein Nitrat-Ion mit der Freisetzung eines Protons verbunden ist.
Die Nitrifikationsgeschwindigkeit ist vom Bodenwassergehalt, dem pH-Wert und der Bodentemperatur abhängig. Bei einer Zunahme der Temperatur von 20 Grad auf 30 Grad verdoppelt sich die Reaktionsgeschwindigkeit der Nitrifikation. Bodenwassergehalte zwischen 40 bis 60 Prozent und ein pH-Wert im neutralen Bereich sind die optimalen Ausgangsbedingungen für die Nitrifikation.
Umwandlungsgeschwindigkeit von Ammonium zum Nitrat in Abhängigkeit von der Temperatur:
- 5°C –► 6 Wochen
- 20°C –► 1 Woche
Als Nebenprodukt kann während des Prozesses der Nitrifikation das klimaschädliche Treibhausgas Lachgas (N2O) in kleinen Mengen freigesetzt werden.
Denitrifikation
Die Denitrifikation bezeichnet die mikrobielle Reduktion von Nitrat (NO3-) über Nitrit (NO2), Stickstoffmonoxid (NO) und Distickstoffmonoxid (N2O) zu elementarem Stickstoff oder Stickoxiden unter anaeroben Bedingungen.
Denitrifikation: NO3--N –► NO2--N –► NO + N2O –► N2
Anaerobe oder fakultativ anaerobe Organsimen wie beispielsweise Bakterien der Gattung Pseudomonas sind für diesen Prozess verantwortlich. Nitrat wird als Sauerstoffquelle bzw. Wasserstoffakzeptor genutzt. Optimale Bedingungen für die Denitrifikation sind eine hohe Wassersättigung des Bodens, Temperaturen zwischen zehn bis 35 Grad und ein pH-Wert im leicht sauren oder leicht alkalischen Bereich. Eine Wassersättigung des Porenraums von 70 bis 80 Prozent führt zu niedrigen Sauerstoffpartialdrücken und fördert die Denitrifikation.
Im Ergebnis einer unvollständigen Denitrifikation können größere Mengen des klimaschädlichen Treibhausgases Lachgas (N2O) freiwerden.
Mineralisation
Die Mineralisation bezeichnet den vollständigen Abbau organischen Substanz durch Mikroorganismen zu mineralischen Verbindungen. Dabei werden die organischen Bestandteile des Bodens unter Bildung von CO2 und Ammonium freigesetzt. Unter warm-feuchten Bedingungen läuft dieser Prozess besonders rasch ab. Bei diesem Vorgang wird Humus abgebaut. Unterschieden wird dabei zwischen schnell mineralisierbarem Humus und Dauerhumus.
Die Bodenbildung seit der Besiedlung der Erde mit Pflanzen und später die landwirtschaftliche Tätigkeit der Menschen haben dazu beigetragen, dass in den Böden große Mengen an Stickstoff organisch gebunden vorliegen. Dieser Vorrat beläuft sich in Mitteleuropa je nach Bodengüte auf Mengen zwischen 3.000 bis 6.000 kg N/ha in null bis 20 cm Ackerkrume (Scheffer und Schachtschabel, 1998). Im Gegensatz zu den mineralischen Stickstoffformen ist organischer Stickstoff nur langsam für die Pflanzen verfügbar. Er ist Bestandteil des Humus im Boden und damit Träger des Bodenlebens.
Immobilisation
Die Festlegung von pflanzenverfügbarem Stickstoff durch physikalische, chemische oder biologische Prozesse wird als Immobilisation bezeichnet. Die Immobilisation von Ammonium-Stickstoff durch Sorption an Bodenpartikeln ist keine oder maximal eine kurzzeitig wirksame Immobilisation, denn das so gebundene Ammonium tritt Schritt für Schritt in die Bodenlösung über, wo es in der Regel rasch zu Nitrat oxidiert wird. Bedeutend kann unter Umständen die biologische Immobilisation sein. Bei dieser nutzen Mikroorganismen die mineralischen Stickstoffquelle für ihre eigene Ernährung und Reproduktion. Sie können dabei so effizient sein, dass schließlich ein Großteil des Mineralstickstoffs kurzfristig in mikrobielle organische Substanz überführt wird.
Allerdings steht dieser Stickstoff nach dem Absterben der Mikroben wieder zur Verfügung und kann durch Mineralisierung erneut pflanzenverfügbar werden.